În mecanica statistica , teoria cinetică a gazelor încearcă să explice comportarea macroscopică a unui gaz pornind de la studiul static al particulelor componente.
Această teorie a fost verificată experimental de către Albert Einstein în 1905.
Gazul este considerat ca fiind alcătuit din moleculele mono- sau poliatomice, care sunt supuse la anumite interacțiuni și anume: interacțiunile electromagnetice(cum ar fi fortele van der Waals), ciocnirile dintre particule și dintre particule și pereții recipientului care conține gazul.
Se fac următoarele aproximări:
- dimensiunile moleculelor sunt neglijabile în raport cu distanțele dintre acestea;
- interacțiunile dintre molecule sunt neglijabile, cu exceptia ciocnirilor reciproce
Relația dintre viteză și presiune
Dacă descompunem viteza unei molecule după cele trei axe:
atunci concentația de particule (molecule pe unitatea de volum) este:
 .
.
Dar, conform teoremei lui Pitagora:
deci
cu
și
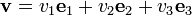
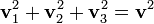

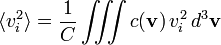

Niciun comentariu:
Trimiteți un comentariu